1 材料与方法
1.1 实验材料与养殖条件
本实验所用褐菖鲉幼鱼来自浙江省海洋水产研究所,为当年人工繁育的幼鱼,平均体长为(5.20±0.38)cm,平均体质量为(4.62±0.92)g。采用活水车将其运抵上海市水产研究所奉贤科研基地后,暂养7 d,暂养池为30 m3水泥池,利用气石曝气增氧,水温为(26.0±0.4) ℃,盐度为20,早、晚投喂以成鳗料兑水自制的软颗粒饲料。
1.2 实验设计
盐度实验分为6、8、10和20(对照)4个盐度梯度组,分别记为S6、S8、S10和S20,每个盐度组对应1个30 m3的水泥池,每个水泥池中放3个聚乙烯网箱作为3个重复,每个重复30尾鱼,网箱规格为100 cm×70 cm×40 cm。实验期间不投饵,随机取样,每个重复每个时间点取样4尾。对于褐菖鲉肠和胃,只取其96 h样品进行消化酶测定;对于肝脏,分别于3、6、12、24、48、96 h进行取样,用于非特异性免疫酶测定。
1.3 样品制备
将实验鱼置于冰盆上解剖,取出胃、肠和肝脏,并剔除附着物,用预冷的生理盐水冲洗干净后,用滤纸吸干,每个重复4尾鱼的胃和肠合成1个样品、4尾鱼的肝脏为另1个样品,分别用于检测胃肠消化酶(胰蛋白酶、胃蛋白酶、淀粉酶和脂肪酶)和肝脏非特异性免疫酶[谷丙转氨酶(Glutamic-pyruvic transaminase,GPT)、谷草转氨酶(Glutamic-oxaloacetic transaminase,GOT)、酸性磷酸酶(Acid phosphatase,ACP)和碱性磷酸酶(Alkaline phosphatase,AKP)]活性,将制备好的样品放置于-80 ℃冰箱保存,待测。测定酶活力前,先将冷冻样品置于4 ℃冰箱解冻,放入预冷的离心管中,加入9倍体积预冷生理盐水,冰浴匀浆,在eppendorf centrifuge 5810R高速冷冻离心机中4 ℃、2 500 r/min离心10 min,取上清液,用于各酶活测定。
1.4 消化酶和非特异性免疫酶活性测定
采用南京建成生物工程研究所生产的试剂盒测定褐菖鲉的胃肠消化酶和肝脏非特异性免疫酶的活性。
1.5 数据处理和统计
数据以平均值±标准差(
2 结果与分析
2.1 盐度胁迫下褐菖鲉幼鱼胃肠消化酶活性的变化
2.1.1 盐度胁迫下褐菖鲉胃肠胰蛋白酶活性的变化
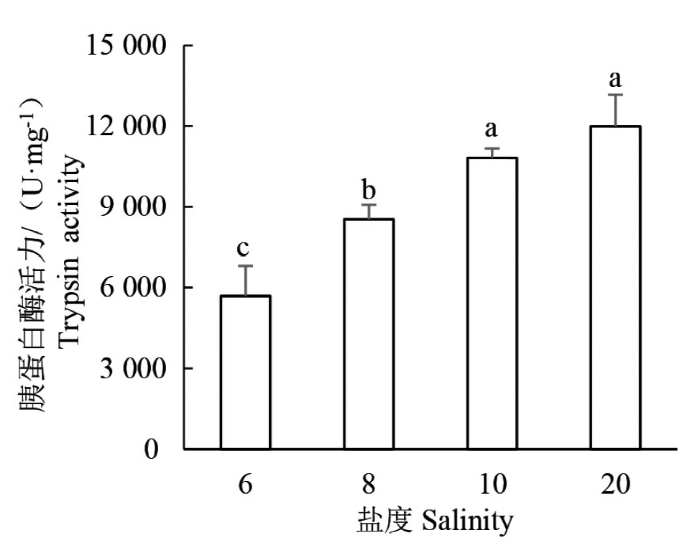
由图1可知,当盐度胁迫96 h时,褐菖鲉幼鱼胃肠胰蛋白酶活性随盐度的升高而升高,其中S6组胰蛋白酶活性为(5 684.30±1 125.31)U·mg-1;S10和S20组胰蛋白酶活性分别为(10 816.89±353.71)、(11 988.96±1 174.22)U·mg-1,均显著高于S6和S8组(P<0.05)。由此可见,S20组胰蛋白酶活性最高,而S6组胰蛋白酶活性最低。
图1
图1
不同盐度下褐菖鲉幼鱼胃肠胰蛋白酶活性
注:不同小写字母表示不同盐度组之间存在显著差异(P<0.05);相同字母表示无显著差异(P>0.05)。
Fig.1
The trypsin activity in the intestine and stomach of juvenile S. marmoratus at the different salinity level
Notes: Different small letters indicated significant differences at the different salinity level (P<0.05); the same small letter indicated no significant difference (P>0.05).It’s the same as in
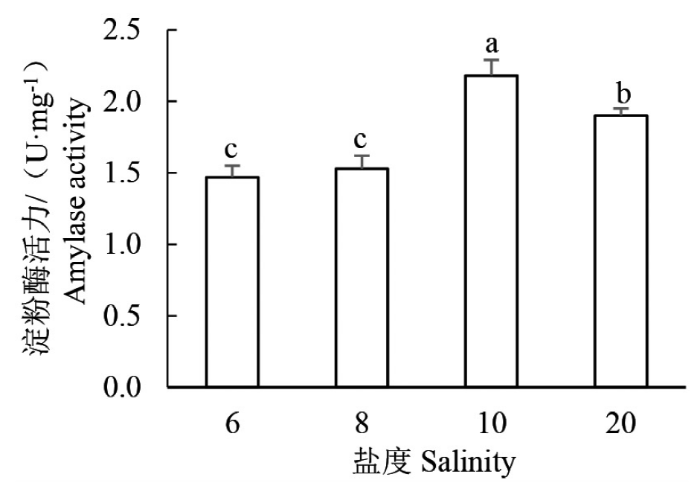
2.1.2 盐度胁迫下褐菖鲉胃肠淀粉酶活性的变化
图2
图2
不同盐度下褐菖鲉幼鱼胃肠淀粉酶活性
Fig.2
The amylase activity in the intestine and stomach of juvenile S. marmoratus at the different salinity level
2.1.3 盐度胁迫下褐菖鲉胃肠胃蛋白酶活性的变化
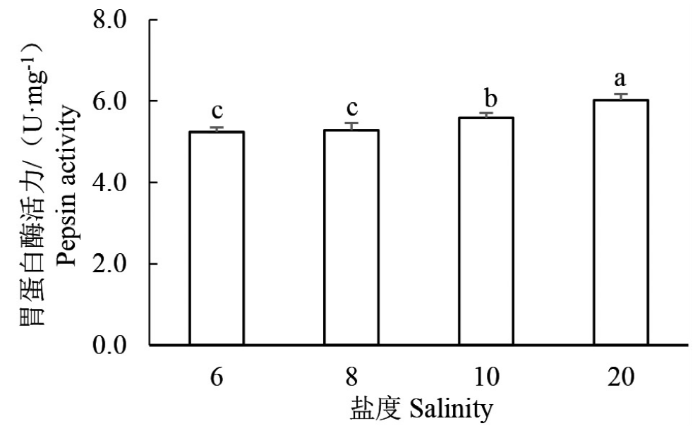
由图3可知,当盐度胁迫96 h时,褐菖鲉幼鱼胃肠胃蛋白酶活性随盐度的升高而升高,其中S6组和S8组胃蛋白酶活性分别为(5.24±0.11)、(5.28±0.18)U·mg-1;S10和S20组胃蛋白酶活性分别为(5.59±0.12)、(6.02±0.15)U·mg-1,均显著高于S6和S8组(P<0.05)。由此可见,S20组胃蛋白酶活性最高,而S6组胃蛋白酶活性最低。
图3
图3
不同盐度下褐菖鲉幼鱼胃肠胃蛋白酶活性
Fig.3
The pepsin activity in the intestine and stomach of juvenile S. marmoratus at the different salinity level
2.1.4 盐度胁迫下褐菖鲉胃肠脂肪酶活性的变化
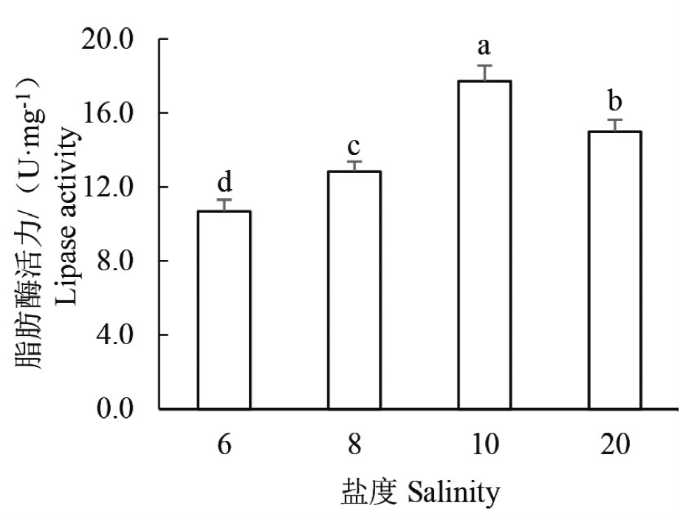
由图4可知,当盐度胁迫96 h时,褐菖鲉幼鱼胃肠脂肪酶活性随盐度的升高呈先上升后下降的趋势,不同盐度组的脂肪酶活性均存在显著差异(P<0.05),其中S10组脂肪酶活性为(17.71±0.84)U·mg-1,显著高于其他组(P<0.05);S6和S8组脂肪酶活性分别为(10.68±0.63)和(12.83±0.54)U·mg-1;S20组脂肪酶活性为(14.98±0.65)U·mg-1,显著高于S6和S8组(P<0.05)。由此可见,S10组脂肪酶活性最高,而S6组脂肪酶活性最低。
图4
图4
不同盐度下褐菖鲉幼鱼胃肠脂肪酶活性
Fig.4
The lipase activity in the intestine and stomach of juvenile S. marmoratus at the different salinity level
2.2 盐度胁迫下褐菖鲉肝脏非特异性免疫酶活性的变化
2.2.1 盐度胁迫下褐菖鲉肝脏GPT活性的变化
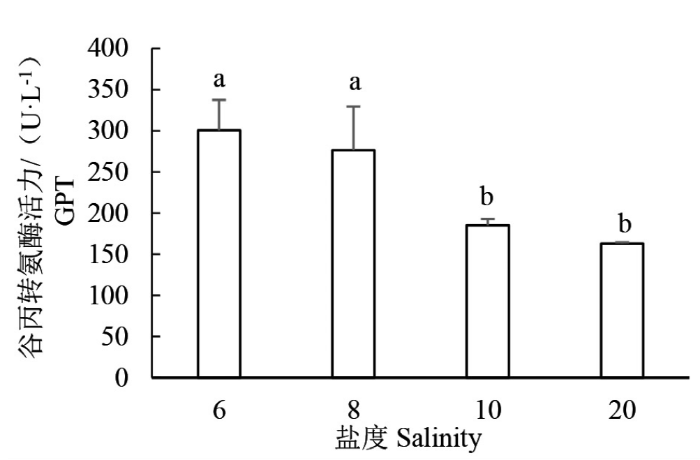
由图5可知,当盐度胁迫96 h时,褐菖鲉幼鱼肝脏GPT活性随盐度的升高呈下降趋势,其中S6组GPT活性为(300.51±36.79) U·L-1,与S8组[(276.32±53.02)U·L -1]无显著性差异(P>0.05);S10和S20组GPT活性别为(184.93±8.05)、(162.93±1.66)U·L-1,显著低于S6和S8组(P<0.05)。由此可见,S6组GPT活性最高,而S20组GPT活性最低。
图5
图5
不同盐度下褐菖鲉幼鱼谷丙转氨酶活性
Fig.5
The glutamic-pyruvic transaminase activity in liver of juvenile S. marmoratus at the different salinity level
2.2.2 盐度胁迫下褐菖鲉肝脏GOT活性的变化
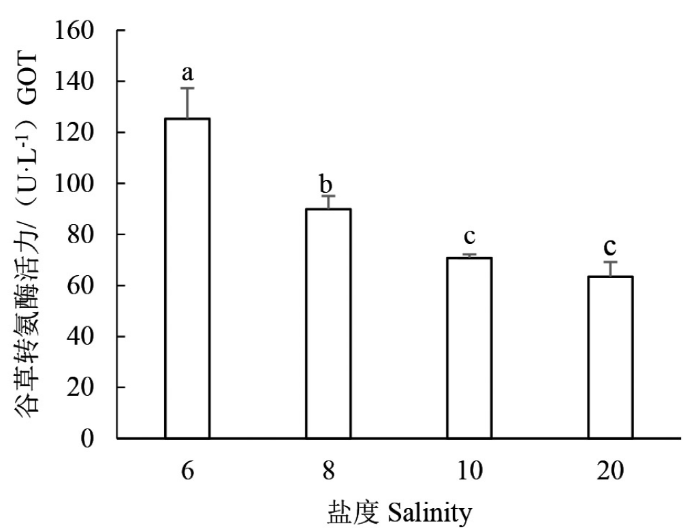
图6可见,当盐度胁迫96 h时,褐菖鲉幼鱼肝脏GOT活性随盐度的升高呈下降趋势,其中S6组GOT活性为(125.38±11.96) U·L-1,显著高于S8组[(89.91±5.20)U·L-1](P<0.05);S10和S20组GOT活性分别为(70.73±1.44)、(63.38±5.84)U·L-1,均显著低于S6和S8组(P<0.05)。 由此可见,S6组GOT活性最高,而S20组GOT活性最低。
图6
图6
不同盐度下褐菖鲉幼鱼谷草转氨酶活性
Fig.6
The glutamic-oxaloacetic transaminase activity in liver of juvenile S. marmoratus at the different salinity level
2.2.3 盐度胁迫下褐菖鲉肝脏ACP活性的变化
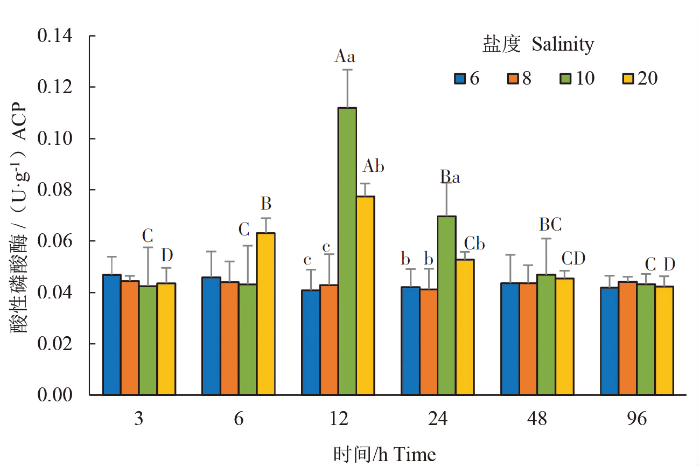
由图7可知,S6、S8组ACP活性在不同时间点均无显著性差异(P>0.05)。S10、S20组ACP活性均呈先上升后下降趋势,其中S10、S20组ACP活性在12 h分别为(0.11±0.02)、(0.08±0.01)U·g-1,均显著高于其他时间组(P<0.05);24 h的S10组ACP活性为(0.07±0.01)U·g-1,显著高于3 、6 、96 h(P<0.05),而48、96 h又逐步降至初始水平,与3、6 h的无显著性差异(P>0.05);6、12 h的S20组ACP活性分别为(0.06±0.01)、(0.08±0.01)U·g-1,均显著高于其他时间组(P<0.05),24 h为(0.05±0.00)U·g-1,显著高于3、96 h(P<0.05),而与48 h[(0.05±0.00)U·g-1]无显著性差异(P>0.05)。由此可见,S10和S20组的ACP活性最高值均出现在盐度胁迫12 h。
图7
图7
盐度胁迫对褐菖鲉幼鱼肝酸性磷酸酶活性的影响
注:不同大写字母表示同一盐度不同时间点之间存在显著差异(P<0.05);不同小写字母表示同一时间点不同盐度组之间存在显著差异(P<0.05);相同字母或未标注字母的表示无显著差异(P>0.05)。
Fig.7
Effects of low salinity on the liver ACP activity of juvenile S. marmoratus
Notes: Different capital letters indicated significant differences in the same salinity level but with different time(P<0.05); different small letters indicated significant differences in the same time but with different salinity levels(P<0.05); the same letters or unlettered letters indicated no significant difference (P>0.05). It’s the same as in
同一时间点,12 h的S10和S20组ACP活性显著高于S6和S8组(P<0.05),且S10组的ACP活性也显著高于S20组(P<0.05);24 h的S10组ACP活性显著高于其他组(P<0.05)。由此可见,S10组ACP活性在盐度胁迫12 h和24 h均显著高于其他盐度组。
2.2.4 盐度胁迫下褐菖鲉肝脏AKP活性的变化
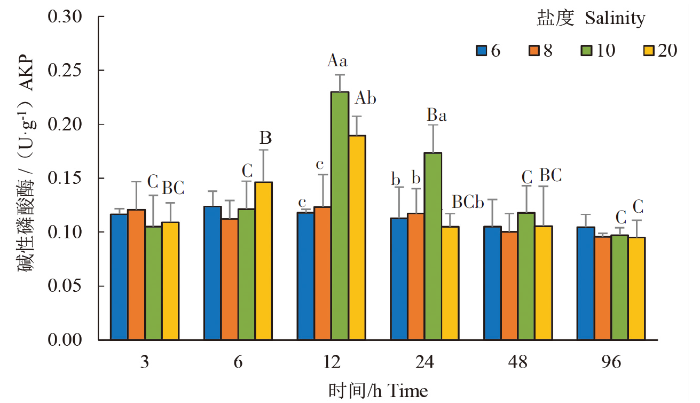
由图8可见,S6和S8组AKP活性在不同时间点均无显著性差异(P>0.05)。S10和S20组AKP活性均呈先上升后下降趋势,其中12、24 h的S10组AKP活性别为(0.23±0.02)、(0.17±0.03)U·g-1,均显著高于其余时间组(P<0.05),且12 h最高,显著高于24 h(P<0.05),48、96 h又逐步降至初始水平,与3、6 h无显著性差异(P>0.05);12 h的S20组AKP活性为(0.19±0.02)U·g-1,显著高于其余时间组(P<0.05),6 h[(0.15±0.03)U·g-1]显著高于96 h[(0.10±0.02)U·g-1],但与3、24、48 h无显著性差异(P>0.05)。由此可知,在不同时间点, S10和S20组AKP活性均在盐度胁迫12 h最高,均显著高于其他时间点。
图8
图8
盐度胁迫对褐菖鲉幼鱼肝碱性磷酸酶活性的影响
Fig.8
Effects of low salinity on the liver AKP activity of juvenile S. marmoratus
同一时间点,12 h的S10和S20组AKP活性显著高于S6和S8组,且S10组的AKP活性也显著高于S20组(P<0.05);24 h的S10组AKP活性显著高于其余3组(P<0.05)。由此可知,S10组AKP活性在盐度胁迫12 h和24 h均最高。
3 讨论
3.1 盐度对褐菖鲉幼鱼胃肠消化酶活性的影响
盐度对鱼类的存活和生长发育具有重要影响[5],其变化会打破鱼类体内的生理生化平衡,从而对它们正常的生命活动产生影响[6]。消化酶主要是由消化腺和消化系统分泌的具有促进作用的酶类[7],可反映鱼体基本消化生理特征[8]。鱼类的消化酶活性会受到盐度变化的影响[9],而且当消化酶活性提高时,鱼类对盐度变化的适应能力也会增强[10]。支兵杰等[11]研究了5、10、15和20四个盐度梯度对大麻哈鱼(Oncorhynchus keta Walbaum)消化酶活性的影响,结果表明在适宜盐度10时,其脂肪酶和蛋白酶活性达到最高;李希国等[12] 研究发现,在盐度为20~30时,黄鳍鲷(Sparus latus)幼鱼的淀粉酶、蛋白酶和脂肪酶活性均显著高于盐度5~15;相智巍等[13]在珍珠龙胆石斑鱼(Epinephelus fuscoguttatus♀×E. lanceolatus♂)消化酶活性研究中,设置了10、15、20、25、30和35六个盐度梯度,结果显示在盐度20和25时,珍珠龙胆石斑鱼幼鱼肠道的胰蛋白酶和脂肪酶活性显著高于盐度10和35。本试验研究结果与上述结果类似,S10和S20组胰蛋白酶、胃蛋白酶、淀粉酶和脂肪酶均显著高于S6和S8组(P<0.05),表明盐度10~20可以提高褐菖鲉幼鱼的消化酶活性。
3.2 盐度对褐菖鲉幼鱼肝脏非特异性免疫酶的影响
ACP是溶菌酶的标志酶,主要参与磷酸酯的代谢,能识别、吞噬和降解入侵的病毒或细菌,起到免疫防护的作用[14]。AKP是溶酶体酶的重要组成部分,参与对外来病原体的分解消化,在非特异免疫反应中发挥重要作用[15],可作为反映鱼体应激和胁迫的指示因子[16]。在低盐胁迫后,鱼体会产生一系列的应激和保护反应,其中包括通过提高ACP和AKP活性,以增强机体的免疫力,这在钝吻黄盖鲽(Pleuronectes yokohama)[14]、军曹鱼(Rachycentyon canadum)[17]和宝石鲈(Scortum barcoo)[5]等研究中均已被证实。此外,在盐度胁迫下,仿刺参(Apostichopus japonicus) ACP 和 AKP 活性呈先升高后降低的趋势[18]。本研究中,S10和S20组ACP和AKP活性也呈先上升后下降趋势,均在12 h达到峰值,之后又逐渐降低并恢复至初始水平,说明盐度胁迫对褐菖鲉幼鱼产生了一定的应激作用,并且在一定程度上激发了免疫反应;而S6和S8组的ACP和AKP活性均无显著性差异(P>0.05),可能是因为更低的盐度胁迫损伤了褐菖鲉幼鱼的免疫系统,从而降低了免疫反应水平,这与钝吻黄盖鲽[14]和军曹鱼[17]的研究结论相似。
4 结论
综上所述,在本实验条件下,盐度10~20可以提高褐菖鲉幼鱼的消化能力和非特异性免疫能力,因此褐菖鲉幼鱼的养殖适宜盐度范围为10~20。
参考文献
Metabolic responses to salinity acclimation in juvenile shortnose sturgeon Acipenser brevirostrum
[J].
淡水与海水养殖的暗纹东方鲀(Takifugu obscurus)幼鱼的生长、生化指标和消化酶活力的差异
[J].本文通过比较暗纹东方鲀(Takifugu obscurus)幼鱼在淡水与海水养殖期间的个体生长指标,测定消化酶和非特异性免疫酶活性、肌肉生化组分,探讨淡水养殖对其生长和生理的影响。结果表明,淡、海水养殖的暗纹东方鲀幼鱼的体长、体质量增长受养殖水盐度的影响极显著(P<0.01),淡水组幼鱼生长指标优于海水组;淡水组暗纹东方鲀幼鱼钠-钾ATP酶(Na<sup>+</sup>/K<sup>+</sup>-ATPase)活力显著小于海水组,溶菌酶(LZM)活力显著大于海水组(P<0.05);抗氧化酶活力、消化酶活力和肌肉生化组分在淡、海水组之间无显著差异(P>0.05)。相较于海水养殖,淡水养殖更有利于暗纹东方鲀的生长。本研究结果可以为暗纹东方鲀淡水规模化健康养殖提供科学数据。
Rapid decreases in salinity,but not increases,lead to immune dysregulation in Nile tilapia, Oreochromis niloticus (L.)
[J].Rapid changes in salinity, as with other environmental stressors, can have detrimental effects on fish and may trigger increased susceptibility to disease. However, the precise mechanisms of these effects are not well understood. We examined the effects of sudden increases or decreases in salinity on teleost immune function using Nile tilapia, Oreochromis niloticus (L.), as the fish model in a battery of bioassays of increasing immune system specificity. Two different salinity experiments were performed: one of increasing salinity (0 to 5, 10 and 20 g L(-1) ) and one of decreasing salinity (20 to 15, 10 and 5 g L(-1) ). Histopathology of anterior kidney, gills, gonads, intestines and liver of exposed fish was performed, but no remarkable lesions were found that were attributable to the salinity treatment regimes. The spleen was removed from each fish for analysis of cytokine expression, and peripheral blood was used for haematology, cortisol and phagocytosis assays. In the increasing salinity experiments, no significant changes were observed in any immune system assays. However, in the decreasing salinity experiments, lymphopenia, neutrophilia and monocytosis were observed in the peripheral blood without modification of the packed cell volume, plasma protein or plasma cortisol levels. Phagocytosis was increased in response to decreases in salinity from 20 g L(-1) to 15 g L(-1), 10 g L(-1) and 5 g L(-1), whereas phagocytic index was not significantly altered. Transforming growth factor-β (TGF-β) transcription increased during the same decreases in salinity. However, the TGF-β value at 5 g L(-1) was less than those in the 15 and 10 g L(-1) salinity treatments. Interleukin-1β (IL-1β) transcription did not significantly respond to either salinity regime. In total, acute salinity changes appeared to trigger reactive dysregulation of the immune response in tilapia, a situation which, when combined with additional co-occurring stressors such as sudden changes in temperature and/or dissolved oxygen, could make fish more susceptible to infectious diseases. Accordingly, these findings may help to explain how sudden environmental changes may initiate disease outbreaks and lead to critical declines in cultured or wild fish populations.© 2012 Blackwell Publishing Ltd.
Effects of salinity on digestive protease activity in the euryhaline sparid Sparus aurata L.: a preliminary study
[J].
低盐胁迫对钝吻黄盖鲽幼鱼鳃Na+/K+-ATP酶、肝脏抗氧化酶和非特异免疫酶的影响
[J].
投喂频率对工厂化循环水养殖珍珠龙胆石斑鱼生长和血浆抗应激酶活力的影响
[J].在水温(29.96 ± 0.40)℃条件下,选用人工配合饲料饲养初始体质量为(291.79 ±59.94) g 的珍珠龙胆石斑鱼,经过60 d 的养殖试验,研究了不同投喂频率1次/ d 、2次/ d、1次/2 d 对工厂化循环水养殖系统中珍珠龙胆石斑鱼生长和血浆抗应激酶活力的影响。结果表明:投喂频率为1次/ 2 d 的成活率(99.39 ± 0.01 ) %,均显著高于投喂频率为1次/ d的(96.75 ±0.66) % 和2次/ d 的(97. 08 ±0.66) % (P < 0.05 ) ; 各试验组间的特定生长率(SGR= 1.05 ~ 1.19 % /d )、肥满度(CF = 1. 63 ~ 1. 77 ) 、相对增质量(RWG = 187. 65% ~205.04% )、日增质量(DWG =4. 33 ~5. 00 g /d ) 、体质量变异系数(SV = 14. 50 ~ 18. 30 )、日摄食率(FI= 1.07 ~ 1.2 4 % /d ) 、饲料转化效率(FCE =81.77% ~ 87. 38% ) 及饲料系数(FCR = 1.15 - 1. 25 ) 均无显著影响(P > 0. 05 ) ; 在血浆抗应激酶活力方面,投喂频率对珍珠龙胆石斑鱼血浆中的碱性磷酸酶(AKP =8. 07 -8.2 6 金氏单位/ 100 mL )、过氧化氢酶(CAT =1.92 ~2.52 U/m L )及超氧化物歧化酶(SOD=23. 39 ~24.34 U/m L ) 也均无显著影响(P >0.05 )。在本试验条件下,可以采用1次/ 2 d 的投喂频率来提高工厂化循环水养殖珍珠龙胆石斑鱼的成活率。